#Produkttrends
Forschungsfortschritte im Zusammenhang mit dem CLDN18.2-Ziel
Hintergrund – Claudin18.2-Protein
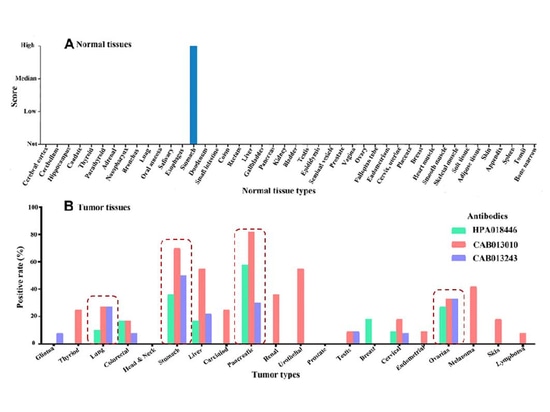
Die CLDN-Proteinfamilie besteht aus mindestens 27 Transmembranproteinen, die anhand ihrer Sequenz in zwei Typen eingeteilt werden können: klassische und nichtklassische. CLDN18 gehört zum nichtklassischen Typ. Das von CLDN18 exprimierte Protein unterliegt Spleißmodifikationen, was zu zwei Subtypen führt: CLDN18.1 und CLDN18.2. CLDN18.2 ist ein hochselektives Markerprotein, das hauptsächlich in differenzierten Epithelzellen der Magenschleimhaut in normalen Geweben exprimiert wird. Bei bösartigen Gewebeerkrankungen zeigt CLDN18.2 jedoch eine entsprechende Expression, insbesondere bei Tumoren des Verdauungstrakts wie Magenkrebs, Bauchspeicheldrüsenkrebs, Speiseröhrenkrebs, Gallengangskrebs und Gallenblasenkrebs. Das Vorhandensein von CLDN18.2 wurde auch in Eierstockkrebs- und Lungenkrebsgeweben nachgewiesen [1–4].
Laut Statistik weisen etwa 33 bis 37 % der Patienten mit soliden Tumoren eine hohe Expression von CLDN18.2 auf. Darüber hinaus hat eine Studie gezeigt, dass bei Magenkrebspatienten etwa 16 bis 73 % der Personen positiv auf die CLDN18.2-Expression getestet wurden [5].
CLDN18.2 und Magenkrebs
Derzeit gibt es erhebliche Unterschiede bei den gemeldeten Positivitätsraten des Claudin18.2-Proteins bei Magenkrebspatienten, was auf Unterschiede in der ethnischen Zugehörigkeit, den Reagenzien und den Nachweiskriterien zurückzuführen sein könnte. Rohde et al. [6] fanden unter Verwendung des CLAUDETECT™18.2-Assays mit denselben Positivitätskriterien eine positive Expressionsrate von 52 % bei japanischen Magenkrebspatienten. Dottermusch et al. [7] verwendeten einen Anti-Claudin18.2-Antikörper von ABCAM zum Nachweis einer kaukasischen Population, verwendeten ein Gewebebewertungssystem als Kriterium für eine positive Expression und berichteten über eine Positivitätsrate von 42,2 % bei Magenkrebsfällen. Baek et al. [8] verwendeten in einer koreanischen Population, die den ABCAM-Anti-Claudin18.2-Antikörper verwendete, eine semiquantitative Bewertungsmethode mit einem Wert von 3 (51 % bis 100 % Färbung) als Kriterium für eine positive Expression und gemäß diesem Standard 29,4 % der Patienten zeigten einen positiven Ausdruck. Xu et al. [9] zeigten in ihrer Studie mit pathologischen Proben von 105 Patienten mit fortgeschrittenem Magen-Siegelringzellkarzinom eine positive Expressionsrate von Claudin18.2 von 95,2 % (100/105), deutlich höher als bei normalen Patienten mit Magen-Adenokarzinom. Unter den Proben zeigten 64,8 % (68/105) mäßige bis hohe Expressionsniveaus von Claudin18.2, und bei 21,0 % (22/105) der Proben betrug das Expressionsniveau von Claudin18.2 sogar ≥90 %. Die oben genannten Studien deuten auf eine hohe positive Expressionsrate von Claudin18.2 bei Magenkrebspatienten hin, und die Expressionsrate und -intensität korrelieren positiv mit der Malignität. CLDN18.2 ist auf die Behandlung vieler Patienten mit Magenadenokarzinom anwendbar.
CLDN18.2 und Bauchspeicheldrüsenkrebs
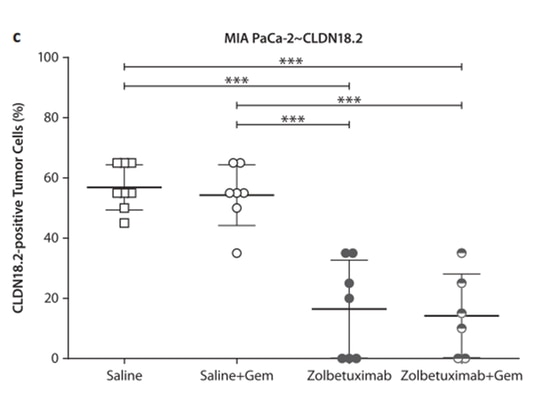
Zusätzlich zu seiner stabil hohen Expression in verschiedenen Magenkrebsgeweben wird CLDN18.2 auch in Bauchspeicheldrüsenkrebsgeweben abweichend exprimiert [11]. Kojima et al. [12] fanden heraus, dass CLDN18 die Tight-Junction-Moleküle in normalen menschlichen Pankreas-Duktal-Epithelzellen über den Proteinkinase-C-Signalweg transkriptionell regulieren kann. In Bauchspeicheldrüsenkrebsgeweben kann CLDN18.2 durch PKC-Aktivatoren und DNA-Methylierungsmodifikationen induziert werden. Studien haben gezeigt [13], dass Gemcitabin (GEM) die Expression von CLDN18.2 in Bauchspeicheldrüsenkrebszellen hochregulieren kann, wodurch die Zolbetuximab-induzierte antikörperabhängige zelluläre Zytotoxizität (ADCC) verstärkt wird. Bei Gemcitabin-resistenten Bauchspeicheldrüsenkrebsarten kann Zolbetuximab das Tumorwachstum verlangsamen und die Metastasierung reduzieren, wodurch das Überleben verlängert wird. Dies unterstützt weiter den möglichen Einsatz von Zolbetuximab als Monotherapie oder in Kombination mit Gemcitabin bei Patienten mit Bauchspeicheldrüsenkrebs, die CLDN18.2 exprimieren.
CLDN18 und hepatozelluläres Karzinom
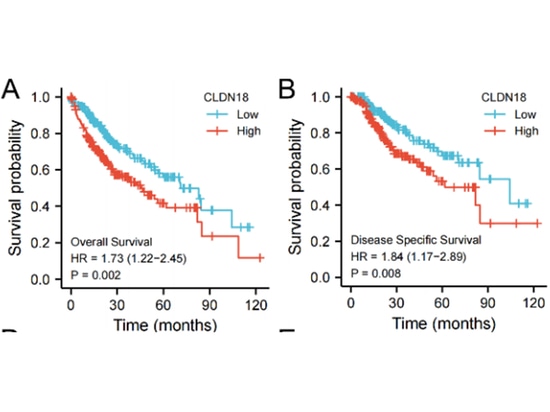
Untersuchungen haben gezeigt [14], dass CLDN18 im Vergleich zu normalen Zellen oder Geweben im hepatozellulären Karzinom (HCC) stark exprimiert wird und mit einer schlechten Überlebensprognose verbunden ist, was als Risikofaktor für das Fortschreiten des HCC dient. CLDN18 weist verschiedene tumorbezogene Funktionen auf und ist an mehreren tumorbezogenen Signalwegen beteiligt. Seine hohe Expression korreliert signifikant mit mehreren klinisch-pathologischen Indikatoren der HCC-Progression und kann die Infiltration von Immunzellen fördern. Die Erstellung von HCC-Diagnose- und Prognosemodellen auf Basis von CLDN18 zeigt einen vielversprechenden Vorhersagewert. Zusammenfassend kann CLDN18 das Fortschreiten des HCC fördern und auf eine schlechte klinische Prognose hinweisen.
Forschung zu anderen zielgerichteten Medikamenten
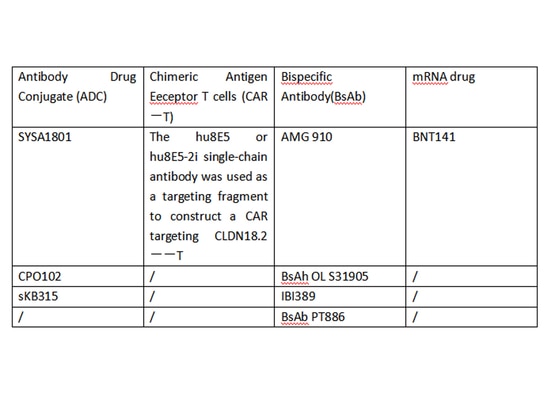
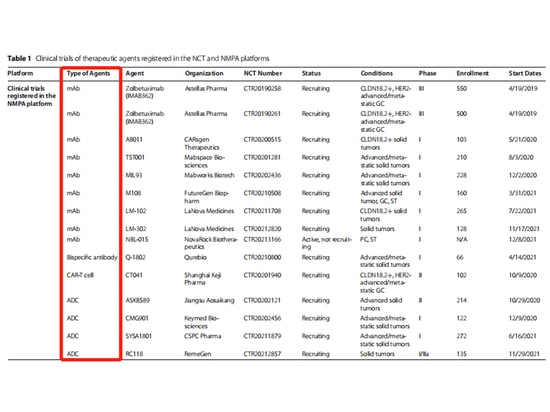
Claudin18.2 zeigt als Pan-Krebs-Ziel eine abnormale Expression in verschiedenen Epitheltumoren und ist zu einem der gefragtesten Ziele in der Krebsforschung geworden. Aktuelle Forschungen zum Targeting von Claudin18.2 umfassen fast alle gängigen Ansätze, einschließlich monoklonaler Antikörper, bispezifischer Antikörper, CAR-T-Zellen und Antikörper-Wirkstoff-Konjugate (ADC). Die Erwartungen an Claudin18.2 sind hoch und er hat das Potenzial, der nächste „PD-1“ zu werden.
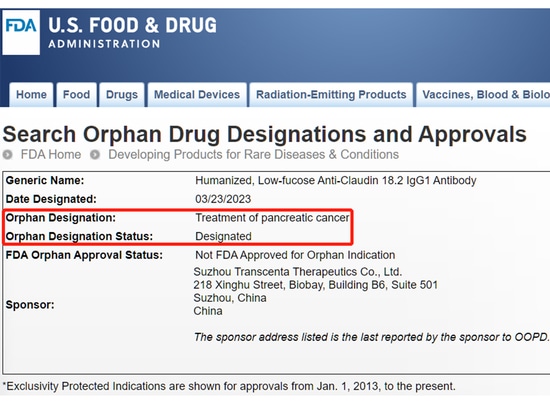
Osemitamab ist ein gegen Claudin18.2 gerichteter Antikörper der zweiten Generation, der derzeit weltweit entwickelt wird. Es handelt sich um einen hochgradig affinitätsoptimierten humanisierten monoklonalen Antikörper gegen Claudin18.2. Osemitamab soll eine verstärkte antikörperabhängige zellvermittelte Zytotoxizität (ADCC) und komplementabhängige Zytotoxizität (CDC) aufweisen.
Erkennungsmethoden
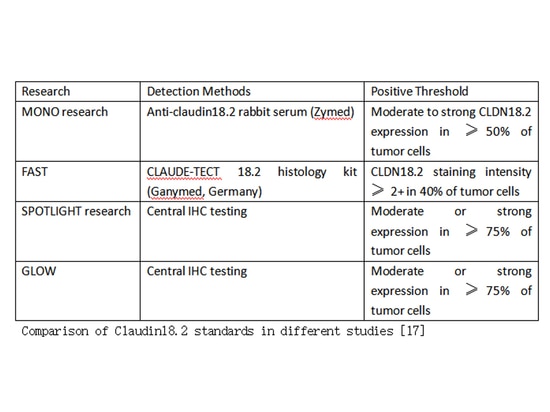
Derzeit ist die Immunhistochemie (IHC) die primäre Methode zum Nachweis der Proteinexpression von CLDN18.2. Es gibt zwei Hauptquellen für etablierte Nachweisantikörper: CLAUDETECT (Ganymed, Deutschland), das in der FAST-Studie verwendet wird, und Abcam (Cambridge, USA). Der CLAUDETECT-Antikörper weist im Vergleich zu den Antikörpern von Abcam eine etwas höhere positive Erkennungsrate auf. Es ist erwähnenswert, dass verschiedene Studien unterschiedliche Schwellenwerte für die Bestimmung der Positivität für Claudin18.2 haben können.
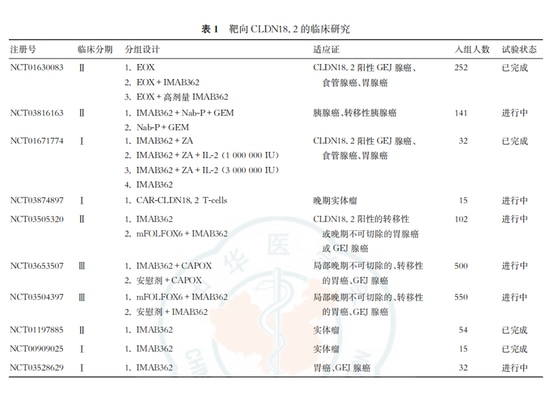
Derzeit basieren die in klinischen Studien für Claudin18.2 verwendeten Nachweismethoden hauptsächlich auf der Immunhistochemie (IHC). Allerdings gibt es in der klinischen Forschung unterschiedliche Kriterien zur Definition des positiven Schwellenwerts und es gibt derzeit keinen einheitlichen Standard. In China nutzen die meisten registrierten Produkte für den Claudin18.2-Nachweis die immunhistochemische Methodik.
Zusammenfassung
Claudin18.2 ist auf der Oberfläche verschiedener Krebszellen weit verbreitet und stellt eine mögliche Lösung dar. Die Kombination des Targetings mit anderen therapeutischen Zielen könnte zusätzliche Vorteile für ein breiteres Spektrum von Patienten bieten.
Referenz:
[1] Antican – cer Res, 2019, 39(12):6973–6979.
[2] The AdV Med 0ncol, 2022, 14: 17588359221083049.
[3] Clin Cancer Res, 2008, 14(23): 7624–7634.
[4] Hi-stol Histopathol, 2022, 37(10): 1031-1040.
[5] Krebserkrankungen (Basel). 18. März 2020;12(3):711.
[6] Jap J Clin Oncol, 2019, 49(9): 870-876.
[7] Virchows Arch, 2019, 475: 563-571.
[8] Anti-Cancer Research, 2019, 39 (12): 6973-6979.
[9] Gastrointest Oncol, 2020, 11(6): 1431-1439.
[10] Forschungsfortschritt des Transmembranproteins CLDN18.2 in der zielgerichteten Krebstherapie
[11] Hi-stol Histopathol, 2022, 37(10): 1031-1040
[12] Ann N Y Acad Sci, 2012, 1257: 85–92
[13] Onkoimmunologie. 10. November 2018;8(1):e1523096.
[14] Die biologische Rolle von CLDN18 beim Fortschreiten des hepatozellulären Karzinoms und sein prognostischer Wert
[15] Biomark Res. 2022 31. Mai;10(1):38.
[16] FDA-Website
[17] Forschungsfortschritt von CLDN18.2 bei Magenkrebs
Haftungsausschluss: Dieser Text dient ausschließlich der Weitergabe und gibt nicht den Standpunkt der Plattform wieder. Wenn es Urheberrechts- oder andere Probleme gibt, kontaktieren Sie uns bitte umgehend und wir werden so schnell wie möglich Korrekturen vornehmen. Danke schön!