Dies ist eine automatisch generierte Übersetzung. Wenn Sie auf den englischen Originaltext zugreifen möchten,
klicken Sie hier
#Produkttrends
{{{sourceTextContent.title}}}
Fujirebio Europe bringt den INNO-LiPA® HCV 2.0 Genotyping Assay auf den Markt, eine effiziente Hilfe für die personalisierte HCV-Therapie
{{{sourceTextContent.subTitle}}}
Fujirebio Europe gab heute die Verfügbarkeit* des INNO-LiPA HCV 2.0 Genotyping Assays bekannt
{{{sourceTextContent.description}}}
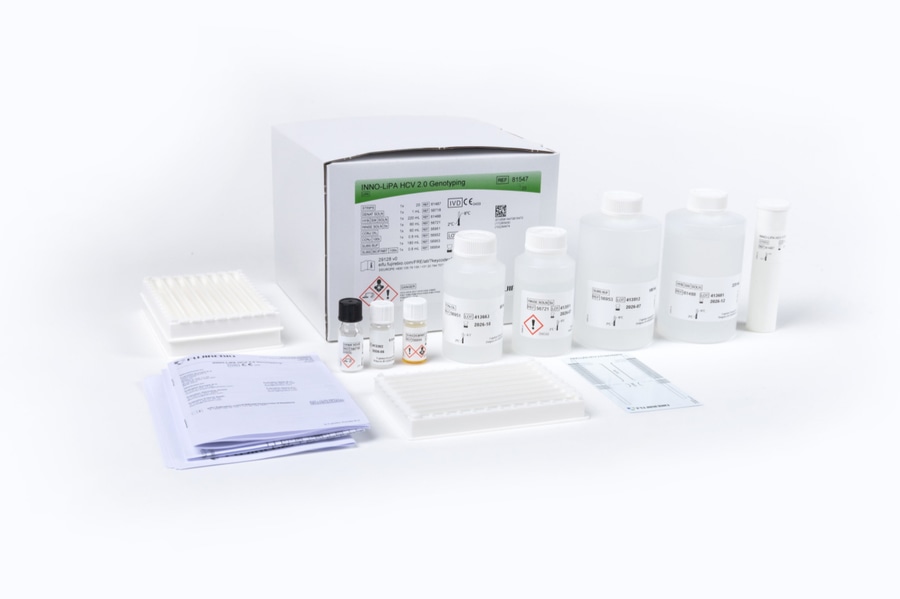
Gent, Belgien - 18. März 2025: Fujirebio Europe gab heute die Verfügbarkeit* des INNO-LiPA HCV 2.0 Genotyping Assays bekannt. Bei dem Produkt, das zuvor von Siemens Healthcare Diagnostics Inc. unter dem Namen VERSANT HCV Genotype 2.0 vertrieben wurde, handelt es sich um einen Zeilensondentest für die In-vitro-Diagnostik, der für den qualitativen Nachweis und die Identifizierung der Hepatitis-C-Virus (HCV)-Genotypen 1 bis 6 sowie der Subtypen a und b des Genotyps 1 in Humanserum- oder EDTA-Plasmaproben entwickelt wurde. In der Mehrzahl der Fälle sind zusätzliche Informationen zum Subtyp verfügbar.
"Bei Fujirebio leisten wir seit den 1990er Jahren mit unserer hochwertigen LiPA-Plattform Pionierarbeit bei molekularen Testlösungen", sagt Christiaan De Wilde, CEO von Fujirebio Europe. "Der historische VERSANT HCV Genotype 2.0 Assay (LiPA) diente als effizientes Hilfsmittel für die personalisierte HCV-Therapie, und wir freuen uns sehr, dass der Test nun offiziell Teil unserer INNO-LiPA-Produktpalette ist. Wir möchten uns bei allen INNO-LiPA-Kunden für ihr anhaltendes Vertrauen bedanken."
Über das Hepatitis-C-Virus
Das Hepatitis-C-Virus ist eine der Hauptursachen für chronische Lebererkrankungen, Leberzirrhose und hepatozelluläres Karzinom (primärer Leberkrebs) und stellt weltweit ein großes Problem für die öffentliche Gesundheit dar. Die HCV-Infektion ist weltweit ungleichmäßig verteilt, wobei die Prävalenz in den einzelnen Ländern und innerhalb der Länder variiert.1
Weltweit sind schätzungsweise 50 Millionen Menschen mit dem chronischen Hepatitis-C-Virus infiziert, wobei es jährlich zu etwa 1,0 Millionen Neuinfektionen kommt. Die WHO schätzt, dass im Jahr 2022 etwa 242 000 Menschen an Hepatitis C sterben werden, vor allem an Zirrhose und Leberzellkarzinom. Eine frühzeitige Erkennung und Behandlung kann schwere Leberschäden verhindern und die Gesundheit langfristig verbessern.2
Über INNO-LiPA HCV 2.0 Genotypisierung
Die INNO-LiPA HCV 2.0 Genotypisierungsprodukte sind IVDR-gekennzeichnet. Die verfügbaren* Produkte sind:
- INNO-LiPA HCV 2.0 Genotypisierung <20T,CE> (Kat# 81547)
- INNO-LiPA HCV 2.0 Amp <20T,CE> (Kat. Nr. 81548)
- INNO-LiPA HCV 2.0 Kontrolle <3T,CE> (Art.-Nr. 81549)
- LiRAS® für LiPA HCV v4 (Kat. Nr. 15228)
Der Assay ist in einer Größe von 20T erhältlich. Der Test kann manuell oder automatisiert (auf dem TENDIGO™ (Kat.-Nr. 80412)) durchgeführt werden und ist nicht als Screening-Test für HCV oder als diagnostischer Test zur Bestätigung des Vorhandenseins von HCV vorgesehen.
Besuchen Sie www.fujirebio.com für weitere Informationen zu diesem Produkt.
* Bitte kontaktieren Sie Fujirebio für weitere Informationen über die lokale Verfügbarkeit des Tests.
Referenzen:
1. Guntipalli P, Pakala R, Kumari Gara S, Ahmed F, Bhatnagar A, Endaya Coronel MK, Razzack AA, Solimando AG, Thompson A, Andrews, K, Enebong Nya G, Ahmad S, Ranaldo R, Cozzolongo R, Shahini E. Worldwide prevalence, genotype distribution and management of hepatitis C. Acta Gastroenterol Belg. 2021 Oct-Dec;84(4):637-656. doi: 10.51821/84.4.015. PMID: 34965046.
2. https://www.who.int/news-room/fact-sheets/detail/hepatitis-c