Automatische Übersetzung anzeigen
Dies ist eine automatisch generierte Übersetzung. Wenn Sie auf den englischen Originaltext zugreifen möchten, klicken Sie hier
#Neues aus der Industrie
{{{sourceTextContent.title}}}
Prostata-Ablationsgeräte sicherer machen
{{{sourceTextContent.subTitle}}}
Die FDA gab Leitlinien heraus, um Empfehlungen für die Gerätehersteller bezüglich der klinischen Prüfung zu geben, die in Übereinstimmung mit speziellen Kontrollen für hochintensive Ultraschallsysteme für Prostatagewebeablationsgeräte durchgeführt werden muss.
{{{sourceTextContent.description}}}
Die FDA hat in diesem Jahr die Sicherheitsbemühungen für Medizinprodukte in mehreren Bereichen verstärkt. In jüngster Zeit hat die Agentur ihre Aufmerksamkeit auf Geräte gerichtet, die zur Ablation von Prostatagewebe entwickelt wurden.
Die Agentur gab am Dienstag einen Leitlinienentwurf heraus, um Empfehlungen für die Gerätehersteller bezüglich der klinischen Prüfung zu geben, die in Übereinstimmung mit speziellen Kontrollen für hochintensive Ultraschallsysteme für Prostatagewebeablationsgeräte durchgeführt werden muss, die unter dem 510(k) Pre-Market Notification Program der Agentur reguliert sind. Dieser Leitlinienentwurf skizziert auch empfohlene klinische Daten zur Unterstützung der Markteinreichung von Geräten zur Ablation von Prostatagewebe, die neuere, innovativere Technologien oder Energieformen zur Ablation (oder Zerstörung) von Prostatagewebe einsetzen.
"Geräte, die Prostatagewebe abtragen oder zerstören, benötigen vor der Vermarktung wichtige Sicherheits- und Wirksamkeitsdaten. Als Teil unseres kontinuierlichen Engagements, die Gerätesicherheit offensiv anzugehen und gleichzeitig Innovationen zu fördern, um Patienten die sichersten und effektivsten Behandlungsmöglichkeiten zu bieten, geben wir heute Empfehlungen zu der Art von klinischen Daten, die Hersteller in ihre Marketingunterlagen für Prostatagewebeablationsgeräte aufnehmen sollten", sagte Jeff Shuren, MD, Direktor des Center for Devices and Radiological Health der FDA. "Unser Vorschlag hebt die Verwendung klinischer Beweise im Rahmen des 510(k)-Premarkett-Meldeprogramms hervor. Diese Anleitung fördert auch Sicherheit und Innovation, indem sie die klinischen Beweise klärt, die neue und sichere Wege zur Zerstörung von Prostatagewebe wie Ultraschall oder alternative Technologien unterstützen würden. Für diese Arten von Prostata-Ablationsgeräten verlangt die FDA klinische Tests, um zu zeigen, dass jedes neue Gerät die Patientensicherheit adressiert, indem es nachweist, dass das Gerät kein Gewebe außerhalb des Zielbereichs ablatiert oder beschädigt und dass das Gerät bei der Ablation von Prostatagewebe im Zielbereich genauso effektiv ist wie ein ähnliches Gerät mit gleichem Sicherheitsprofil.
Vor der Einleitung einer klinischen Untersuchung für Prostata-Gewebeablationsgeräte ermutigt die FDA die Hersteller, die FDA mit einer Voranmeldung zu kontaktieren, um detailliertes Feedback über die geplante klinische Untersuchung zu erhalten.
Der Anwendungsbereich dieses Leitlinienentwurfs beschränkt sich auf die klinischen Prüfungen zur Unterstützung der Marktzulassung für allgemeine Indikationen von Ablationssystemen für Prostatagewebe. Dieser Leitlinienentwurf bezieht sich nicht auf die klinischen Prüfungen von Geräten, die zur Behandlung bestimmter Prostatakrankheiten wie Prostatakrebs oder gutartiger Prostatahyperplasie bestimmt sind. Krankheitsspezifische Studien verwenden verschiedene Endpunkte und Studiendesigns, um Sicherheit und Wirksamkeit im Vergleich zu einer Studie zum Nachweis einer effektiven Gewebeablation nachzuweisen.
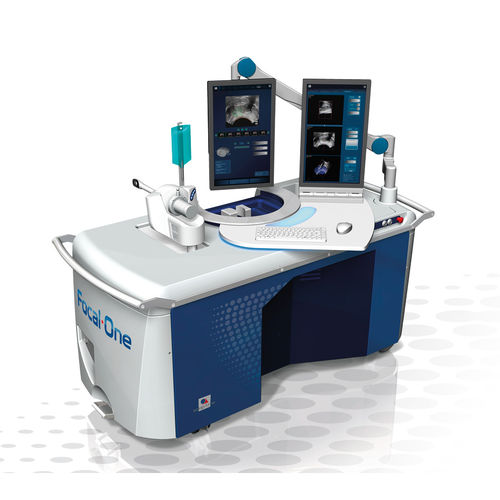
Ein aktuelles Beispiel für diese Art von Technologie ist das Focal One Gerät von EDAP TMS, wie oben abgebildet. Das Gerät nutzt eine fortschrittliche Ultraschalltechnologie, um krankes Gewebe zu erfassen und abzutragen